AUTOR: Santiago Rodríguez de Diego
Las innovaciones en el recubrimiento de comprimidos buscan la modificación de la liberación del fármaco, la mejora de la biodisponibilidad y de la eficacia terapéutica, la reducción de la dosis administrada, de la incidencia de efectos secundarios y de los costes de la terapia, así como brindar beneficios económicos a los fabricantes.
-1687158753.webp)
En la actualidad, los cada vez más estrictos requisitos toxicológicos, medioambientales y de seguridad han conducido a la sustitución progresiva del disolvente orgánico (empleado en el pasado por ofrecer cortos tiempos de procesamiento) por recubrimientos a base de agua. Como solución a los numerosos inconvenientes asociados al uso de disolventes en el recubrimiento farmacéutico, surgieron las técnicas conocidas como “solventless” o “dry coating”, en las cuales se evita o limita en gran medida el uso de disolventes en el material de recubrimiento.
En la última década, se han realizado importantes esfuerzos en el desarrollo del recubrimiento de formas farmacéuticas, como el empleo de modelos probabilísticos para regular aspectos fundamentales del proceso de recubrimiento, la utilización de productos más naturales que permitan mantener toda su funcionalidad, o el desarrollo de innovadores dispositivos caseros de recubrimiento a pequeña escala capaces de ofrecer mejores resultados que las técnicas de recubrimiento convencionales. Estas innovaciones tienen como propósito garantizar y mejorar (en el consumo de energía, distribución de la película, eficiencia del secado y procesamiento continuo) la calidad del producto final. Existe, para el futuro, un enorme margen de desarrollo en el área del recubrimiento de comprimidos para la consecución de beneficios específicos.
Los comprimidos, en todas sus variantes, constituyen la forma de dosificación más popular, llegando a suponer aproximadamente el 70 % del total de medicamentos dispensados (Ubhe & Subscription, 2020).
Figura 1.
Clasificación de los comprimidos farmacéuticos.
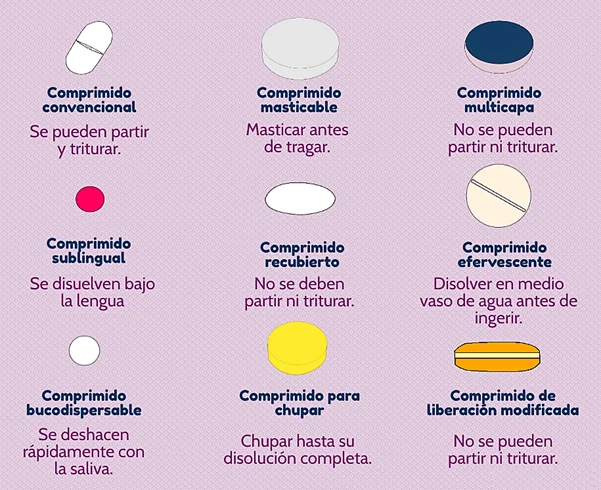
Nota: Esta figura muestra la clasificación de los diferentes tipos de comprimidos farmacéuticos (Fuente: Boticonsejos, 2019).
La finalidad del recubrimiento farmacéutico es: la protección del medicamento del ambiente externo (luz, humedad, aire, etc.), el enmascaramiento de olores y sabores desagradables, facilitar la ingestión, así como la identificación por parte del paciente, el incremento de las propiedades mecánicas del comprimido, la modificación de la liberación del medicamento e introducir dos medicamentos incompatibles dentro de un mismo comprimido.
El recubrimiento se puede formular especialmente para regular la velocidad a la que se disuelve el comprimido y el punto en el que el organismo absorberá las sustancias activas tras la ingestión.
Figura 2.
Proceso de recubrimiento con azúcar (grageado).
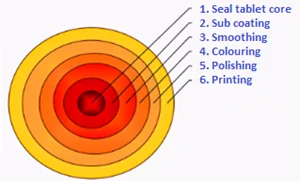
Nota: Esta figura muestra las diferentes etapas del proceso de recubrimiento con azúcar (grageado) (Fuente: Raihan, 2021).
Figura 3.
Proceso de recubrimiento pelicular.
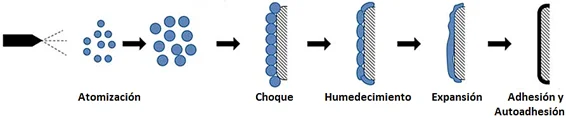
Nota: Esta figura muestra las diferentes etapas del proceso de recubrimiento pelicular (Fuente: Pharmapproach, 2021).
Figura 4.
Proceso de recubrimiento en seco.
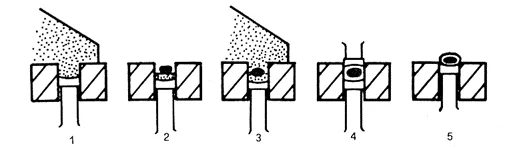
Nota: Esta figura muestra las diferentes etapas del proceso de recubrimiento en seco (Fuente: Spazioinfo, 2007).
Figura 5.
Proceso de microencapsulación.
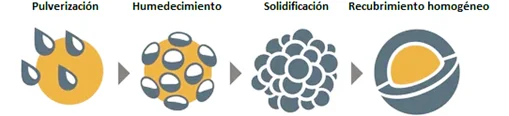
Nota: Esta figura muestra las diferentes etapas del proceso de microencapsulación (Fuente: Shutterstock, n.d.).
Dada la importancia de recubrimiento pelicular, es importante destacar:
Sus formulaciones se componen de: un polímero formador de película, un plastificante, un vehículo apropiado (disolvente) y otros aditivos (colorantes) (Kamble et al., 2011).
Tabla 1.
Polímeros formadores de película empleados en el recubrimiento pelicular.
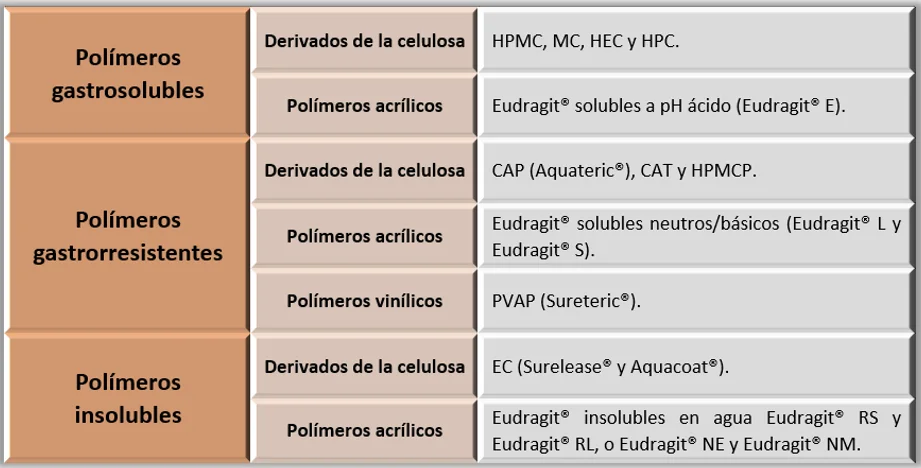
Nota: Esta tabla muestra la clasificación de los distintos polímeros formadores de película empleados en el recubrimiento pelicular (Fuente: Elaboración propia, a partir de: Ciobanu et al., 2021; Lehmann, 1986; Palmieri et al., 2000; Plaizier-Vercammen & Suenens, 1991; Rogers & Wallick, 2011; Shokri & Adibki, 2013; Siepmann et al., 2007; Thakral et al., 2013; Zaid & Qaddomi, 2012).
Por un lado, se encuentran los bombos de recubrimiento, los cuales, a su vez, se dividen en tradicionales y perforados (siendo estos preferibles a los anteriores) (Behzadi et al., 2008). Y, por otro lado, se encuentran los sistemas de lecho fluido, los cuales se clasifican en función de la disposición de la boquilla de pulverización. Distinguiéndose tres tipos: pulverización superior, inferior y tangencial.
Tabla 2.
Procedimientos y equipos empleados en el recubrimiento pelicular.
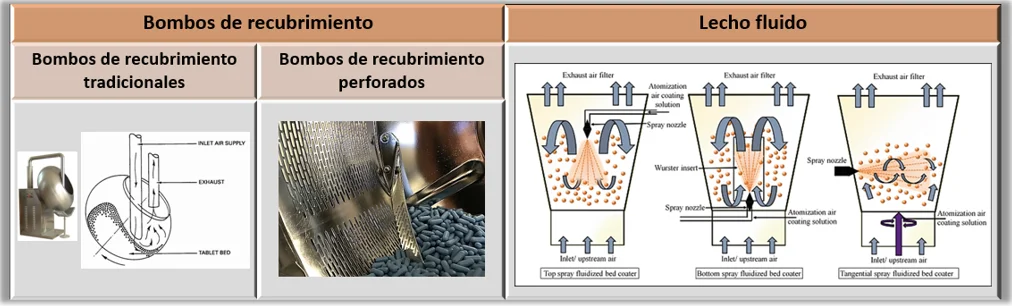
Nota: Esta tabla muestra la clasificación de los distintos procedimientos y equipos empleados en el recubrimiento pelicular (Fuente: Elaboración propia, a partir de: AIPAK Pharmaceutical Equipment, 2023; Freund-Vector, 2018; Vinchhi & Patel, 2022).
El objetivo general de este trabajo de revisión bibliográfica es identificar los métodos más innovadores y útiles de recubrimiento farmacéutico. Además, los objetivos específicos son:
Para la elaboración del presente trabajo de búsqueda bibliográfica se consultaron múltiples fuentes (artículos científicos, revistas científicas, libros, revisiones y patentes). Como principal motor de búsqueda se empleó Google Scholar, además de otros como Elsevier, PubMed, MDPI y la red social ResearchGate. El idioma empleado para la búsqueda fue el inglés. Se delimitaron la temática y las coordenadas de búsqueda introduciendo términos como: “Innovations”, “Innovative”, “Pharmaceutical coating”, etc. combinados entre sí o con otros, y haciendo uso de operadores lógicos o booleanos (and, or, not) y truncamientos mediante la raíz de la palabra. Se acotaron las áreas de conocimiento a Farmacia y Química, buscando publicaciones que pudieran tener alguna aplicación relacionada con la industria farmacéutica. Se estableció como límite temporal los últimos 10 años, y se realizó, además, una búsqueda por autor. Por último, para el diseño o modificación de imágenes se utilizó el programa Paint.
En los últimos años, han surgido una serie de técnicas conocidas como “solventless” o “dry coating” para dar solución a los numerosos inconvenientes asociados al uso de disolventes. Estos métodos de fabricación evitan o limitan en gran medida el uso de disolventes en el material de recubrimiento.
Su clasificación se realiza en función del estado físico de los agentes que forman el recubrimiento cuando se aplican al sustrato (Cerea et al., 2008).
Figura 6.
Técnicas de recubrimiento sin disolventes.
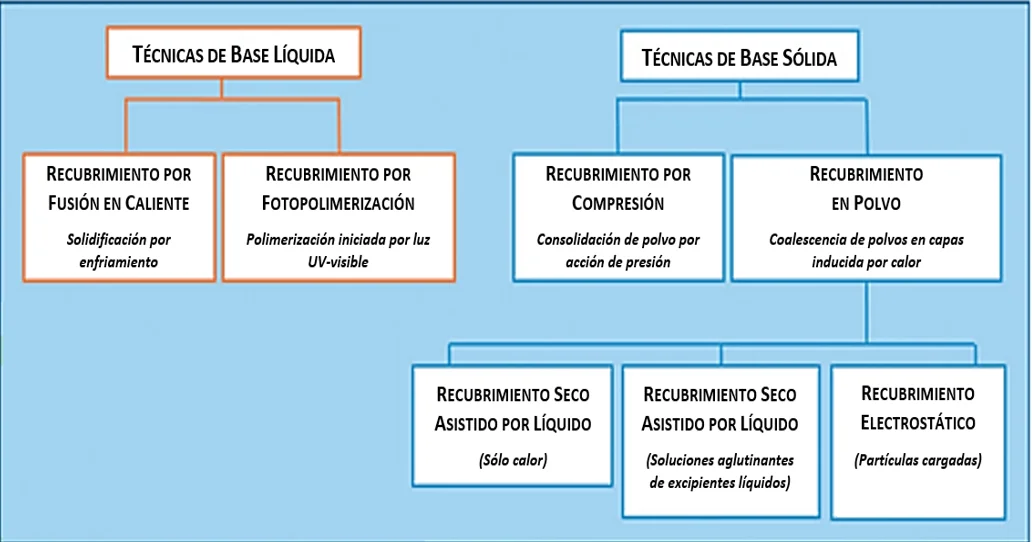
Nota: Esta figura muestra la clasificación de las técnicas de recubrimiento sin disolventes (Fuente: Elaboración propia).
El material de recubrimiento se aplica en estado fluido sobre el sustrato y luego se solidifica por enfriamiento (Achanta et al., 1997).
Esta técnica no requiere de disolvente, y en ella, la elección de los excipientes de recubrimiento depende principalmente de su función en la forma de dosificación. Cabe decir que se trata de un proceso económico.
Se utiliza principalmente para la producción de formulaciones de liberación prolongada (Griffin & Niebergall, 1999; Kennedy & Niebergall, 1998).
Figura 7.
Proceso de recubrimiento por fusión en caliente.
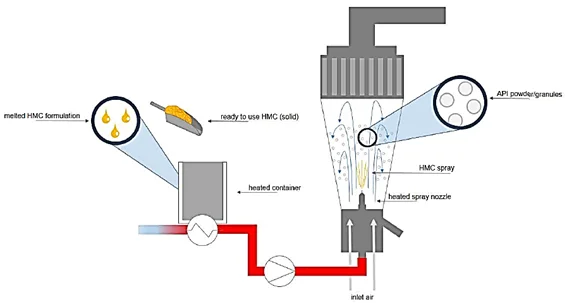
Nota: Esta figura muestra el proceso de recubrimiento por fusión en caliente (Fuente: Raphael Janousek, 2020).
La fotopolimerización o fotocurado es un enfoque químico propuesto para recubrir rápidamente los comprimidos a temperatura ambiente o inferior (Bose & Bogner, 2007). Esta técnica tiene una amplia aplicación en odontología y medicina.
El sistema está compuesto por: una fuente de luz UV visible, materiales fotocurables, un fotoiniciador o fotosensibilizador y un agente formador de poros (Pappas, 1985).
Esta técnica permite la liberación inmediata y prolongada, así como la modificación de la liberación (Bose, 2006).
Figura 8.
Proceso de recubrimiento por fotopolimerización.
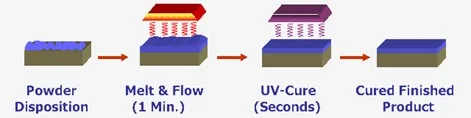
Nota: Esta figura muestra el proceso de recubrimiento por fotopolimerización (Fuente: Lonczak, 2010)
Consiste en la pulverización de pequeñas cantidades de agua o disoluciones acuosas de aglutinante para facilitar, mediante la acción capilar interfacial, la adhesión de las partículas de recubrimiento a la superficie del núcleo (Foppoli et al., 2017).
Esta técnica requiere de muy poca cantidad de líquido dentro de la formulación. El empleo de excipientes (plastificantes) en fase líquida sirve para dar alguna funcionalidad para la formación de la película (Sauer et al., 2013).
Recientemente se ha usado para aplicar HPMC en granulados que contienen probióticos, conduciendo a altas tasas de supervivencia bacteriana (Park et al., 2016).
Figura 9.
Proceso de recubrimiento seco asistido por líquido.
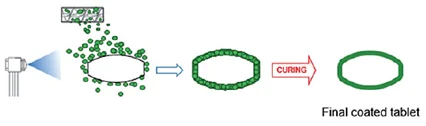
Nota: Esta figura muestra el proceso de recubrimiento seco asistido por líquido (Fuente: Foppoli et al., 2017).
En él tiene lugar la eliminación total de la ayuda líquida, produciéndose un recubrimiento a partir de polvos en capas, originado únicamente mediante el calor (Cerea et al., 2008).
Sus formulaciones poseen un alto grado de diseño, y se componen de: un polímero, un plastificante, un agente antiadherente, colorantes y, en su caso, opacificantes.
Figura 10.
Proceso de recubrimiento de adhesión térmica.
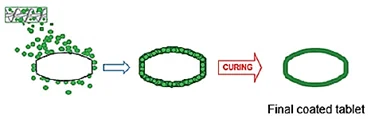
Nota: Esta figura muestra el proceso de recubrimiento de adhesión térmica (Fuente: Foppoli et al., 2017).
Consiste en la deposición de polvo de alta calidad hasta lograr una película uniforme. Ha sido ampliamente utilizado en el recubrimiento de piezas metálicas en el sector de la automoción.
En él, la adhesión de partículas de polvo a sustratos se lleva a cabo mediante las fuerzas electrostáticas. Para ello, se emplea: un campo eléctrico, un sustrato conectado a tierra (Qiao et al., 2010) y polvos capaces de acumular carga (Watanabe et al., 2007).
La carga electrostática de las partículas se puede obtener por tribocarga o carga corona (empleándose más frecuentemente esta última, por la complejidad de la tribocarga) (Lin & Kawashima, 2012; Maroni et al., 2016).
Los factores que influyen en la deposición son: la nebulización de plastificantes en estado líquido al uso de cargas electrostáticas y el voltaje de carga de la pistola electrostática.
Figura 11.
Proceso de recubrimiento electrostático.
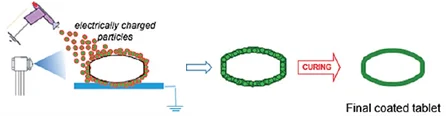
Nota: Esta figura muestra el proceso de recubrimiento electrostático (Fuente: Foppoli et al., 2017).
Modelado del grosor de la capa de recubrimiento farmacéutico. (Madlmeir et al., 2021)
Se llevó a cabo el modelado del grosor de la capa de recubrimiento farmacéutico mediante una combinación de simulaciones de Monte Carlo y CFD-DEM para un proceso de recubrimiento farmacéutico Wurster para microesferas. La combinación de ambos modelos permitía la predicción durante todo el proceso tanto de las distribuciones de masa como del espesor del recubrimiento. Se observó que en la zona de pulverización más cercana a la boquilla cuanto menor era el tamaño de partícula, mayor era el grosor de la capa de recubrimiento. La tasa de pulverización suponía un gran impacto en la variabilidad del recubrimiento entre partículas, frente al flujo de aire. Y, por último, tuvo lugar el desarrollo de un modelo estocástico que permitía investigar la contribución relativa de la variabilidad de la capa de recubrimiento y la variabilidad del peso del relleno frente a la falta de uniformidad del producto en un proceso de llenado de cápsulas de sistemas de gránulos de unidades múltiples (MUPS).
Figura 12.
Ejemplo de sistema de gránulos de unidades múltiples (MUPS).
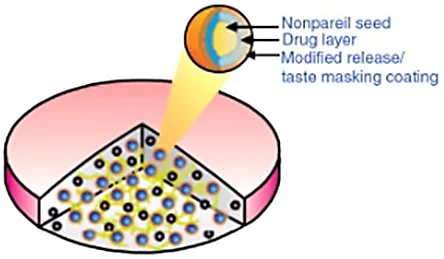
Nota: Esta figura muestra un ejemplo de sistema de gránulos de unidades múltiples (MUPS) (Fuente: Abdul et al., 2010).
Un innovador recubrimiento entérico a base de cera para productos orales farmacéuticos y nutracéuticos. (Habashy et al., 2020)
La alta demanda de productos nutracéuticos con recubrimientos entéricos sin ingredientes artificiales ha conducido al empleo de polímeros de grado GRAS (Generalmente Reconocido como Seguro) (Barbosa, 2017).
Hasta el momento, la aplicación de ceras solo tenía fines estéticos (principalmente abrillantar) (Kelley, 1948). Este trabajo presenta el primer recubrimiento entérico funcional eficiente, completamente natural, mediante una emulsión O/W caliente de ceras naturales en una disolución de alginato de sodio (Alg). Para ello, se emplearon distintos tipos de ceras (cera blanca de abeja, cera amarilla de abeja, cera de ceresina, etc.).
Se crearon emulsiones con distintas proporciones de Alg-cera-GMS y se aplicaron a un núcleo de teofilina anhidra (fármaco idóneo por su baja solubilidad y su relativamente bajo peso molecular). Se evaluaron las propiedades de formación de películas y la homogeneidad y se determinó la proporción ideal de cera para minimizar la absorción de ácido y cumplir con los criterios para el recubrimiento entérico establecidos en la farmacopea. Por último, se comparó con otros sistemas comerciales de recubrimiento de grado GRAS.
Figura 13.
Comprimidos con recubrimiento entérico a base de diferentes ceras naturales.
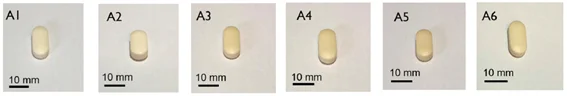
Nota: Esta figura muestra una serie de comprimidos con recubrimiento entérico a base de diferentes ceras naturales (Fuente: Habashy et al., 2020).
Un método de recubrimiento por pulverización para la detección de compuestos en dosis bajas en comprimidos farmacéuticos utilizando imágenes químicas Raman mejoradas en superficie (SER-CI). (Cailletaud et al., 2018)
El recubrimiento farmacéutico con nanopartículas metálicas para los análisis SER-CI presenta una gran dificultad para lograr una cobertura homogénea. La técnica SER-CI permite detectar principios activos o impurezas en concentraciones muy bajas y presenta una mayor sensibilidad y un menor tiempo de adquisición que las imágenes convencionales Raman.
Se desarrolló un nuevo sistema de pulverización casero y portátil, cuyos parámetros óptimos se determinaron mediante diseño de experimentos. Se recubrieron comprimidos de paracetamol con Ag Nps de 3 formas:
Figura 14.
a) Método de deposición por goteo. b) Método de recubrimiento por absorción. c) Nuevo sistema de pulverización casero.
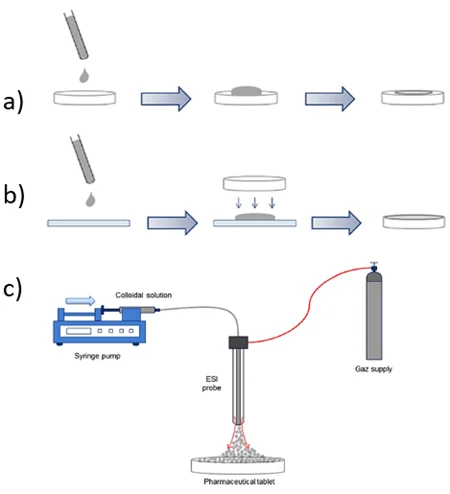
Nota: Esta figura muestra los tres métodos empleados para el recubrimiento de los comprimidos, a saber: a) Método de deposición por goteo. b) Método de recubrimiento por absorción. c) Nuevo sistema de pulverización casero (Fuente: Cailletaud et al., 2018).
Se compararon las 3 técnicas de recubrimiento mediante la realización de estudios de homogeneidad. Primero, aplicando el algoritmo K-means en una imagen SER-CI y luego, se corroboraron los resultados con MALDI MSI.
Figura 15.
a) Aplicación del algoritmo K-means en una imagen SER-CI de comprimidos recubiertos por los tres métodos planteados. b) Representación de la distribución de iones [Ag]+ mediante análisis MALDI-MSI en comprimidos de paracetamol/pvp recubiertos por coloides de plata en los tres métodos planteados.
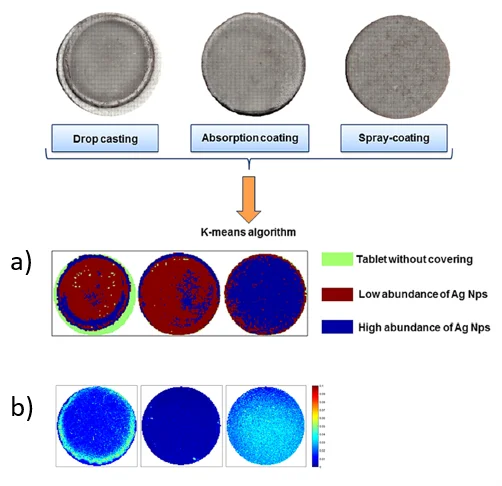
Nota: Esta figura muestra los estudios de homogeneidad realizados, a saber: a) Aplicación del algoritmo K-means en una imagen SER-CI de comprimidos recubiertos por los tres métodos planteados. b) Representación de la distribución de iones [Ag]+ mediante análisis MALDI-MSI en comprimidos de paracetamol/pvp recubiertos por coloides de plata en los tres métodos planteados (Fuente: Cailletaud et al., 2018).
Se observó como el nuevo dispositivo generaba una cobertura homogénea, mientras que con las otras dos técnicas se producía el denominado efecto “anillo de café”.
Además, se realizó un estudio de la reproducibilidad, que determinó que el nuevo dispositivo generaba recubrimientos reproducibles por la ausencia de cambios en la superficie de los comprimidos, mientras que con los métodos tradicionales se producía la disolución de la superficie (generándose poros y grietas) además de una ligera migración.
Tabla 3.
Criterios para la elección de la técnica de recubrimiento adecuada.
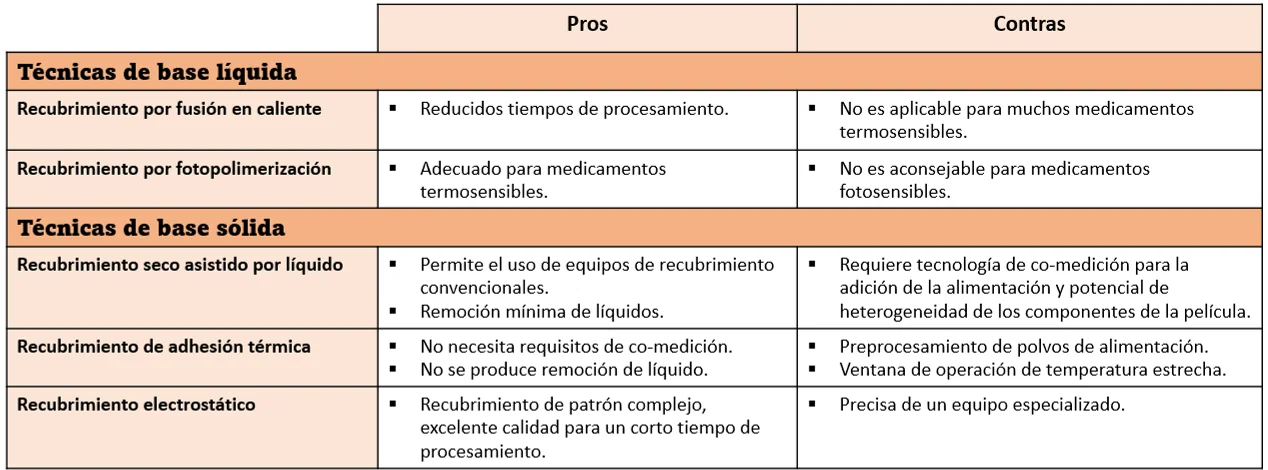
Nota: Esta tabla muestra los criterios a los que hay que atender para la elección de la técnica de recubrimiento adecuada (Fuente: Elaboración propia, a partir de: Sauer et al., 2013).
Modelado del grosor de la capa de recubrimiento farmacéutico. (Madlmeir et al., 2021)
Se desarrolló un enfoque de modelado innovador, mediante simulaciones estocásticas, donde la cantidad de sólido depositado en una sola partícula dependía del número de pasadas a través de la zona de pulverización y de la ganancia de recubrimiento en una sola pasada. Bajas tasas de pulverización suponían un aumento de la uniformidad del producto, del tiempo de ejecución de los procesos y de las pérdidas debido al secado. Una disminución en el tamaño de partícula conducía a un aumento del grosor de la capa de recubrimiento y un aumento del número de partículas, lo que a su vez llevaba a una disminución de la variabilidad del recubrimiento. En futuras investigaciones se deberá ampliar el enfoque de modelado presentado.
Un innovador recubrimiento entérico a base de cera para productos orales farmacéuticos y nutracéuticos. (Habashy et al., 2020)
Se ha desarrollado un nuevo recubrimiento entérico a base de materiales naturales, dando lugar a películas atractivas con propiedades gastrorresistentes. Se determinó la proporción ideal de cera para minimizar la absorción de ácido y cumplir con los criterios para productos de liberación retardada. Este recubrimiento es aplicable en una amplia gama de ceras naturales y ofrece propiedades gastrorresistentes superiores a otros recubrimientos de grado GRAS comerciales. Cabe destacar que la naturaleza no sintética de los componentes constituye una alternativa excelente frente a otros recubrimientos entéricos de grado GRAS.
Un método de recubrimiento por pulverización para la detección de compuestos en dosis bajas en comprimidos farmacéuticos utilizando imágenes químicas Raman mejoradas en superficie (SER-CI). (Cailletaud et al., 2018)
Se ha diseñado un método de recubrimiento por pulverización eficiente frente a la deposición por goteo de sustratos SERS, que permite un control significativo de la deposición de nanopartículas metálicas (gracias a una distribución homogénea). La optimización de los parámetros del sistema (llevada a cabo mediante diseño de experimentos), conduce a una alta reproducibilidad y una fuerte mejora de las señales SERS. La suspensión coloidal permanece en la superficie del comprimido lo que posibilita los análisis SER-CI. No se produce disolución o migración de los compuestos hidrosolubles presentes en el comprimido. Futuras mejoras en el sistema de pulverización deberán ir dirigidas hacia la consecución de un recubrimiento más eficiente de las muestras.
Las innovaciones en el recubrimiento de comprimidos tienen como propósito mejorar las características o propiedades del recubrimiento y, por extensión, del medicamento.
Los cada vez más estrictos requisitos toxicológicos, medioambientales y de seguridad, han conducido a una sustitución gradual de los recubrimientos a base de disolventes orgánicos por recubrimientos a base de agua.
Como solución a los problemas asociados al uso de disolventes, surgieron las técnicas “solventless” o “dry coating”.
El empleo de modelos probabilísticos ha conducido a importantes innovaciones en el recubrimiento farmacéutico.
Las formas de dosificación de liberación prolongada formuladas a partir de partículas recubiertas de pequeño tamaño se difunden más fácilmente en el tracto GI que las partículas gruesas.
En productos nutracéuticos se han sustituido gradualmente los recubrimientos sintéticos por polímeros entéricos de grado GRAS y productos naturales.
Se ha visto que dispositivos innovadores caseros de recubrimiento pueden conducir a mejores resultados que las técnicas de recubrimiento convencionales.
En la última década ha habido importantes avances en este campo, pero aún queda un enorme margen de desarrollo para el futuro.
Abdul, S., Chandewar, A. V., & Jaiswal, S. B. (2010). A flexible technology for modified-release drugs: Multiple-unit pellet system (MUPS). Journal of Controlled Release, 147(1), 2–16.
Achanta, A. S., Adusumilli, P. S., James, K. W., & Rhodes, C. T. (1997). Development of Hot Melt Coating Methods. Drug Development and Industrial Pharmacy, 23(5), 441–449.
AIPAK Pharmaceutical Equipment. (2023). Coating Pan:The Ultimate Buying Guide in 2023. https://www.icapsulepack.com/coating-pan/
Barbosa, J. (2017). Going Natural: Using polymers from nature for gastroresistant applications. British Journal of Pharmacy, 2(1).
Behzadi, S., Toegel, S., & Viernstein, H. (2008). Innovations in Coating Technology. Recent Patents on Drug Delivery & Formulation, 2(3), 209–230.
Bose, S. (2006). Development and evaluation of solventless photocurable pharmaceutical film coating. University of Connecticut.
Bose, S., & Bogner, R. H. (2007). Solventless photocurable film coating: Evaluation of drug release, mechanical strength, and photostability. AAPS PharmSciTech, 8(3), E42–E51.
Boticonsejos, I. (2019). Tipos de comprimidos y formas de administración. Boticonsejos - Consejos Desde La Farmacia. https://boticonsejos.es/tipos-de-comprimidos-y-formas-de-administracion/
Cailletaud, J., Bleye, C. De, Dumont, E., Sacré, P. Y., Gut, Y., Bultel, L., Ginot, Y. M., Hubert, P., & Ziemons, E. (2018). Towards a spray-coating method for the detection of low-dose compounds in pharmaceutical tablets using surface-enhanced Raman chemical imaging (SER-CI). Talanta, 188(June), 584–592.
Cerea, M., Zema, L., Palugan, L., & Gazzaniga, A. (2008). Recent developments in dry coating. Pharmaceutical Technology Europe, 20(2), 40–44.
Ciobanu, N., Guranda, D., Ciobanu, C., & Petrache, A. (2021). Current assortment of gastro-soluble polymers used in pill coating and film application methods. Internauka, 187(11).
Foppoli, A. A., Maroni, A., Cerea, M., Zema, L., & Gazzaniga, A. (2017). Dry coating of solid dosage forms: an overview of processes and applications. Drug Development and Industrial Pharmacy, 43(12), 1919–1931.
Freund-Vector. (2018). Freund-Vector’s Perforated Coating Pans. https://www.freund-vector.com/freund-vectors-perforated-coating-pans/
Grekov, M. A., & Kostyrko, S. A. (2015). A multilayer film coating with slightly curved boundary. International Journal of Engineering Science, 89, 61–74.
Griffin, E. N., & Niebergall, P. J. (1999). Release Kinetics of a Controlled-Release Multiparticulate Dosage Form Prepared Using a Hot-Melt Fluid Bed Coating Method. Pharmaceutical Development and Technology, 4(1), 117–124.
Habashy, R., Khoder, M., Zhang, S., Pereira, B., Bohus, M., Tzu-Wen Wang, J., Isreb, A., & Alhnan, M. A. (2020). An innovative wax-based enteric coating for pharmaceutical and nutraceutical oral products. International Journal of Pharmaceutics, 591, 119935.
Kamble, N. D., Chaudhari, P. S., Oswal, R. J., Kshirsagar, S. S., & Antre, R. V. (2011). Innovations in Tablet Coating Technology: A Review. International Journal of Applied Biology and Pharmaceutical Technology, 2(1), 214–218.
Kelley, W. C. (1948). The use of a Microcrystalline Wax in Tablet Polishing. II. Journal of the American Pharmaceutical Association (Scientific Ed.), 37(8), 332.
Kennedy, J. P., & Niebergall, P. J. (1998). Evaluation of Extended-Release Applications for Solid Dispersion Hot-Melt Fluid Bed Coatings Utilizing Hydrophobic Coating Agents. Pharmaceutical Development and Technology, 3(1), 95–101.
Lehmann, K. (1986). In Wasser dispergierbare, hydrophile Acrylharze mit abgestufter Permeabilität für diffusionsgesteuerte Wirkstoffabgabe aus Arzneiformen. Acta Pharmaceutica Technologica, 32(3), 146–152.
Lin, S.-Y., & Kawashima, Y. (2012). Current status and approaches to developing press-coated chronodelivery drug systems. Journal of Controlled Release, 157(3), 331–353.
Lonczak, R. (2010). UV-Curable Powder Coatings For Heat Sensitive Substrates. Coatings Tech. https://www.dvuv.com/uv-curable-powder-coatings-for-heat-sensitive-substrates/
Madlmeir, S., Forgber, T., Trogrlic, M., Jajcevic, D., Kape, A., Contreras, L., Carmody, A., Liu, P., Davies, C., Sarkar, A., & Khinast, J. G. (2021). Modeling the coating layer thickness in a pharmaceutical coating process. European Journal of Pharmaceutical Sciences, 161(February), 105770.
Maroni, A., Zema, L., Cerea, M., Foppoli, A., Palugan, L., & Gazzaniga, A. (2016). Erodible drug delivery systems for time-controlled release into the gastrointestinal tract. Journal of Drug Delivery Science and Technology, 32, 229–235.
Nokhodchi, A., & Farid, D. (2002). Microencapsulation of paracetamol: By various emulsion techniques using cellulose acetate phthalate. Pharmaceutical Technology North America, 26(6), 54–60.
Palmieri, G. F., Michelini, S., Di Martino, P., & Martelli, S. (2000). Polymers with pH-dependent solubility: Possibility of use in the formulation of gastroresistant and controlled-release matrix tablets. Drug Development and Industrial Pharmacy, 26(8), 837–845.
Pappas, S. P. (1985). UV curing by radical, cationic and concurrent radical-cationic polymerization. Radiation Physics and Chemistry (1977), 25(4–6), 633–641.
Park, H. J., Lee, G. H., Jun, J.-H., Son, M., Choi, Y. S., Choi, M.-K., & Kang, M. J. (2016). Formulation and in vivo evaluation of probiotics-encapsulated pellets with hydroxypropyl methylcellulose acetate succinate (HPMCAS). Carbohydrate Polymers, 136, 692–699.
Pharmapproach. (2021). Tablet Coating Process: Film Coating. In Pharmaceutical Technology. https://www.pharmapproach.com/tablet-coating-process-film-coating-2/
Plaizier-Vercammen, J., & Suenens, G. (1991). Evaluation of Aquateric, a pseudolatex of cellulose acetate phthalate, for its enteric coating properties on tablets. STP Pharma Sciences, 1, 307–312.
Qiao, M., Zhang, L., Ma, Y., Zhu, J., & Chow, K. (2010). A novel electrostatic dry powder coating process for pharmaceutical dosage forms: Immediate release coatings for tablets. European Journal of Pharmaceutics and Biopharmaceutics, 76(2), 304–310.
Raihan, R. (2021). Tablet coating process. Coating Process of Tablets. https://www.slideshare.net/roshaankharotai/coating-process-of-tablets
Raphael Janousek, M. S. (2020). A Quality by Design Approach for an Immediate Release Hot Melt Coating (HMC) Formulation with Taste Masking Properties. BIOGRUND. https://www.biogrund.com/wp-content/uploads/2020/07/Whitepaper-.-BonuWax-QbD.pdf
Rogers, T. L., & Wallick, D. (2011). Reviewing the use of ethylcellulose, methylcellulose and hypromellose in microencapsulation. Part 2: Techniques used to make microcapsules. Drug Development and Industrial Pharmacy, 37(11), 1259–1271.
Sauer, D., Cerea, M., DiNunzio, J., & McGinity, J. (2013). Dry powder coating of pharmaceuticals: A review. International Journal of Pharmaceutics, 457(2), 488–502.
Shokri, J., & Adibki, K. (2013). Application of Cellulose and Cellulose Derivatives in Pharmaceutical Industries. In Cellulose - Medical, Pharmaceutical and Electronic Applications.
Shutterstock. (n.d.). Microencapsulation - the Scheme of Creating a Composite Product - Microcapsules - Vector Illustration. Retrieved February 17, 2023, from https://www.shutterstock.com/es/image-vector/microencapsulation-scheme-creating-composite-product-microcapsules-1010517751
Siepmann, F., Hoffmann, A., Leclercq, B., Carlin, B., & Siepmann, J. (2007). How to adjust desired drug release patterns from ethylcellulose-coated dosage forms. Journal of Controlled Release, 119(2), 182–189.
Spazioinfo. (2007). Rivestimento Di Compresse. Corso Di Impianti Dell’industria Farmaceutica. http://win.spazioinfo.com/public/RIVESTIMENTO COMPRESSE 2006-2007.pdf
Thakral, S., Thakral, N. K., & Majumdar, D. K. (2013). Eudragit®: A technology evaluation. Expert Opinion on Drug Delivery, 10(1), 131–149.
Ubhe, T., & Subscription, C. (2020). A Brief Overview on Tablet and It’s Types. Journal of Advancement in Pharmacology, 1(1), 21–31.
Vinchhi, P., & Patel, M. M. (2022). Optimization of Tablet Coating (pp. 103–133).
Watanabe, H., Ghadiri, M., Matsuyama, T., Ding, Y., Pitt, K., Maruyama, H., Matsusaka, S., & Masuda, H. (2007). Triboelectrification of pharmaceutical powders by particle impact. International Journal of Pharmaceutics, 334(1–2), 149–155.
Zaid, A. N., & Qaddomi, A. (2012). Development and stability evaluation of enteric coated Diclofenac sodium tablets using Sureteric. Pakistan Journal of Pharmaceutical Sciences, 25(1), 59–64.

¡Muchas gracias!
Hemos recibido correctamente tus datos. En breve nos pondremos en contacto contigo.